Durante años, el cáncer y el Alzheimer han sido dos de los diagnósticos más temidos en medicina. Sin embargo, múltiples estudios epidemiológicos han identificado un fenómeno curioso: rara vez aparecen en la misma persona. Ahora, una nueva investigación experimental en ratones plantea una hipótesis sorprendente: algunos tumores podrían enviar señales biológicas que ayudan al cerebro a eliminar proteínas tóxicas asociadas con el Alzheimer.
Diversos análisis poblacionales han mostrado que las personas con cáncer tienen menos probabilidades de desarrollar Alzheimer, y que quienes padecen Alzheimer presentan menor riesgo de cáncer, incluso tras ajustar factores como la edad.
Aunque esta relación inversa ha sido observada durante años, los mecanismos biológicos detrás del fenómeno no estaban claros. El nuevo estudio aporta una posible explicación molecular.
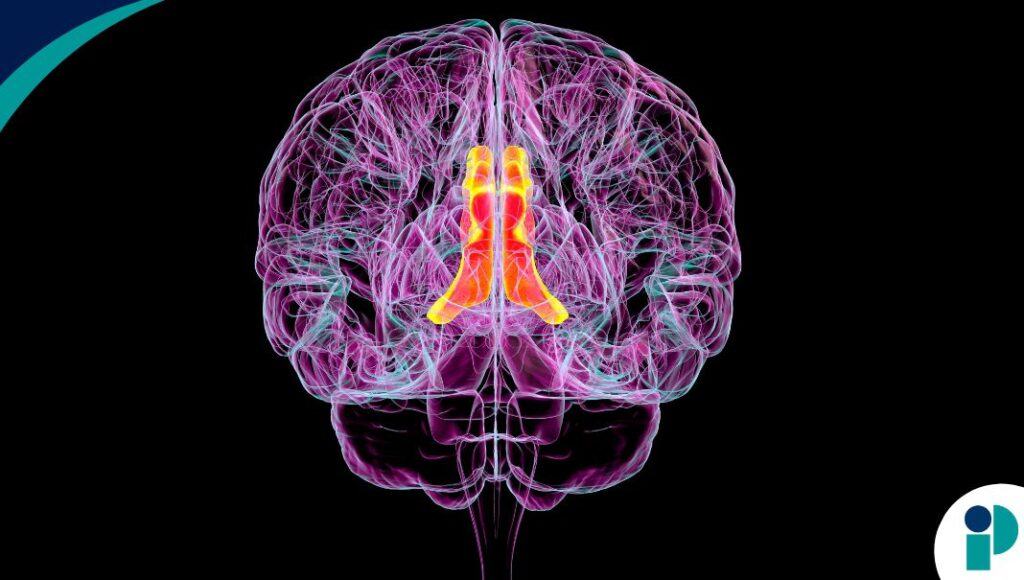
Cómo se forma el Alzheimer en el cerebro
El Alzheimer se caracteriza por la acumulación de placas de beta amiloide, depósitos pegajosos de proteínas que se agrupan entre las neuronas. Estas placas:
- Interfieren en la comunicación neuronal
- Desencadenan inflamación
- Provocan daño progresivo del tejido cerebral
- Deterioran la memoria y el pensamiento
En modelos animales diseñados para desarrollar estas placas, la acumulación suele aumentar con la edad, replicando un rasgo clave de la enfermedad humana.
Para investigar la relación, los científicos implantaron tumores humanos de pulmón, próstata y colon bajo la piel de ratones modificados para desarrollar Alzheimer. El resultado fue inesperado:
- Los cerebros de los ratones con tumores dejaron de acumular placas de beta amiloide.
- En algunos casos, los animales mostraron mejorías en la memoria frente a los ratones sin tumores.
Esto sugería que el efecto no solo era microscópico, sino también funcional.
La proteína clave: cystatin-C
El equipo rastreó el fenómeno hasta una proteína llamada cystatin-C, liberada por los tumores al torrente sanguíneo.
Según el estudio:
- La cystatin-C puede cruzar la barrera hematoencefálica.
- Una vez en el cerebro, se une a pequeños cúmulos de beta amiloide.
- Actúa como una “marca” que señala estas proteínas para su eliminación.
Activación de las células limpiadoras del cerebro
El proceso involucra a la microglía, células inmunitarias residentes del cerebro encargadas de eliminar desechos y proteínas mal plegadas.
En el Alzheimer:
- La microglía pierde eficiencia.
- Las placas se acumulan y se endurecen.
En los ratones con tumores:
- La cystatin-C activó un sensor llamado Trem2 en la microglía.
- Esto cambió su comportamiento hacia un estado más agresivo de limpieza.
- El resultado fue una mayor eliminación de placas.
A primera vista, la idea de que el cáncer pueda “proteger” al cerebro resulta contradictoria. Sin embargo, la biología suele funcionar mediante compensaciones.
Los investigadores plantean que:
- La secreción de cystatin-C es parte de la biología tumoral.
- Su efecto protector sería un subproducto no intencional.
Esto no significa que el cáncer sea beneficioso, sino que revela rutas biológicas potencialmente aprovechables en terapias.
El “sube y baja” entre degeneración y crecimiento celular
La investigación se suma a la hipótesis de un “balancín biológico”:
- Los mecanismos que favorecen la supervivencia y proliferación celular (como en cáncer)
- Podrían oponerse a los que conducen a degeneración neuronal
La cystatin-C aportaría una evidencia física de esta relación. Los autores advierten que los hallazgos aún están lejos de aplicarse en humanos:
- Los modelos murinos no replican toda la complejidad del Alzheimer humano.
- No se sabe si los tumores en pacientes producen suficiente cystatin-C.
- Tampoco si esta llega al cerebro de la misma forma.
Implicaciones terapéuticas futuras
Pese a las limitaciones, el descubrimiento abre nuevas líneas de investigación:
Posibles estrategias:
- Fármacos que imiten la acción de la cystatin-C.
- Versiones bioingenierizadas de la proteína.
- Moléculas que activen la vía Trem2 en la microglía.
El objetivo sería potenciar la capacidad natural del cerebro para eliminar proteínas tóxicas sin necesidad de un tumor. El estudio también subraya la interconexión del cuerpo humano:
Un tumor en pulmón o colon puede:
- Liberar moléculas al torrente sanguíneo.
- Cruzar barreras protectoras.
- Modificar el comportamiento de células cerebrales.
Un mensaje de esperanza desde la investigación
Aunque estos hallazgos no cambiarán el tratamiento inmediato de pacientes con cáncer o Alzheimer, sí aportan una perspectiva alentadora.
Comprender enfermedades graves en profundidad puede revelar mecanismos inesperados útiles para otras patologías.
La lección más contundente es que los procesos biológicos rara vez son simples: una proteína perjudicial en un órgano puede convertirse en una herramienta protectora en otro.
Fuente original aquí