La Administración de Alimentos y Medicamentos (FDA) propuso excluir ciertos medicamentos para la pérdida de peso de una lista clave de compuestos farmacéuticos, una decisión que podría restringir su producción a gran escala por parte de instalaciones subcontratadas.
De aprobarse, la medida afectaría principalmente a empresas de telesalud, que dependen de estas instalaciones para elaborar versiones de medicamentos a partir de sustancias a granel, y fortalecería los esfuerzos de compañías como Novo Nordisk y Eli Lilly frente a imitaciones no autorizadas.
Sin necesidad clínica de subcontratación
El regulador señaló que no existe una necesidad clínica para que terceros elaboren versiones compuestas de medicamentos como:
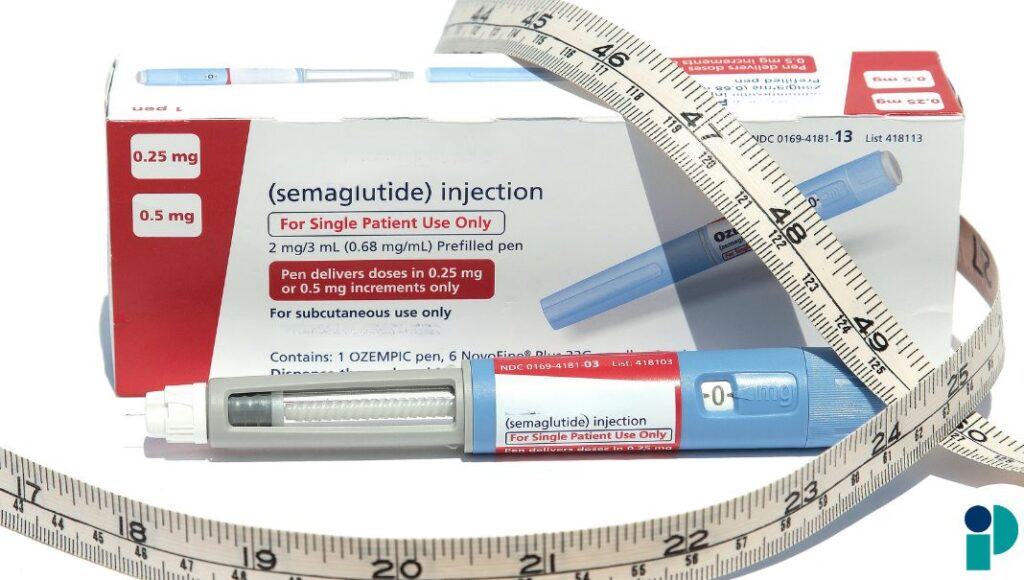
- Semaglutida (presente en Ozempic y Wegovy)
- Tirzepatida (comercializada como Mounjaro y Zepbound)
- Liraglutida, una molécula más antigua
Según la FDA, estos fármacos no requieren ser producidos mediante formulación magistral, un proceso en el que farmacias combinan ingredientes para crear versiones personalizadas o alternativas.
Uso limitado y regulado
La formulación magistral es legal en situaciones específicas, como:
- Escasez de medicamentos
- Necesidades individuales del paciente (por efectos secundarios o ajustes de dosis)
Sin embargo, la FDA enfatizó que este mecanismo debe ser una excepción limitada, no una práctica extendida para replicar medicamentos comerciales.
Muchas empresas de telesalud utilizan dos esquemas:
- Farmacias 503A: preparan medicamentos personalizados por paciente
- Instalaciones 503B: producen medicamentos compuestos a gran escala
Expertos señalan que la exclusión de estos fármacos de la lista 503B podría no alterar significativamente la formulación personalizada, pero sí limitar la producción masiva.
Consulta pública en curso
La FDA abrió un periodo para recibir comentarios públicos hasta el 29 de junio, antes de tomar una decisión final sobre esta propuesta.
La iniciativa busca reforzar la regulación sobre medicamentos para la obesidad, limitar la producción no autorizada y garantizar que estos tratamientos se mantengan dentro de los estándares de seguridad y eficacia establecidos.