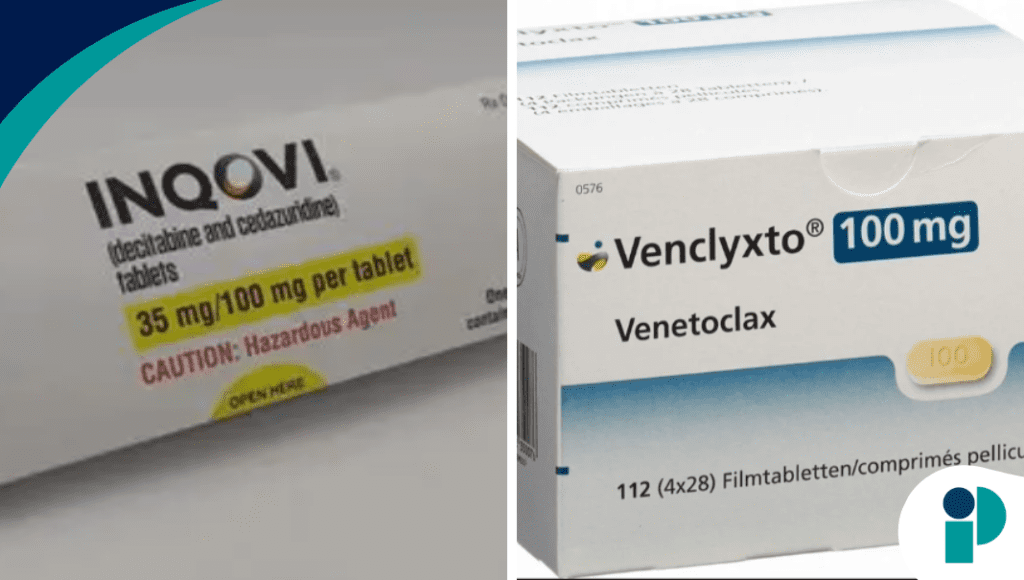
La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) aprobó la combinación oral de decitabina/cedazuridina y venetoclax para adultos con leucemia mieloide aguda (LMA) recién diagnosticada que no pueden recibir quimioterapia intensiva debido a la edad o comorbilidades.
La autorización posiciona a este esquema como una nueva alternativa terapéutica para pacientes mayores de 75 años o con condiciones médicas complejas, al ofrecer un tratamiento completamente oral que podría reducir la necesidad de infusiones y facilitar el manejo ambulatorio.
Los resultados del estudio fase 2 ASCERTAIN-V mostraron que la combinación alcanzó una tasa de respuesta completa de hasta 46.5%, con una mediana de respuesta de aproximadamente dos meses. Además, 80% de los pacientes que lograron respuesta completa se mantuvieron libres de progresión durante al menos seis meses.
Otro de los hallazgos destacados fue una supervivencia global mediana de 15.5 meses, un dato considerado relevante en pacientes con LMA que no son candidatos a terapias intensivas convencionales.
El esquema aprobado combina Inqovi (decitabina/cedazuridina) con Venclexta (venetoclax), consolidando una estrategia terapéutica basada en hipometilantes y bloqueo de BCL-2, utilizada cada vez más en hematología oncológica.
Aunque el tratamiento mostró beneficios clínicos importantes, los investigadores también reportaron efectos adversos frecuentes, incluyendo anemia, neutropenia febril y disminución de plaquetas, eventos comunes en este tipo de terapias hematológicas.
Especialistas señalaron que esta aprobación podría redefinir el estándar terapéutico en pacientes con leucemia mieloide aguda no aptos para quimioterapia intensiva, especialmente por la posibilidad de ofrecer un manejo menos invasivo y más accesible fuera del entorno hospitalario.
Fuente original aquí