La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) aceptó la solicitud de nuevo fármaco (NDA) para brepocitinib, un inhibidor dual de TYK2/JAK1, propuesto para el tratamiento de la dermatomiositis, y otorgó a la solicitud revisión prioritaria, una designación reservada para terapias que podrían representar avances clínicos relevantes en enfermedades graves.
La agencia estableció una fecha objetivo de decisión bajo la Ley de Tarifas de Medicamentos Recetados (PDUFA) para el tercer trimestre de 2026. De recibir la aprobación regulatoria, Priovant Therapeutics prevé lanzar el medicamento en Estados Unidos hacia finales de septiembre de 2026.
Dermatomiositis: una enfermedad con necesidades terapéuticas no cubiertas
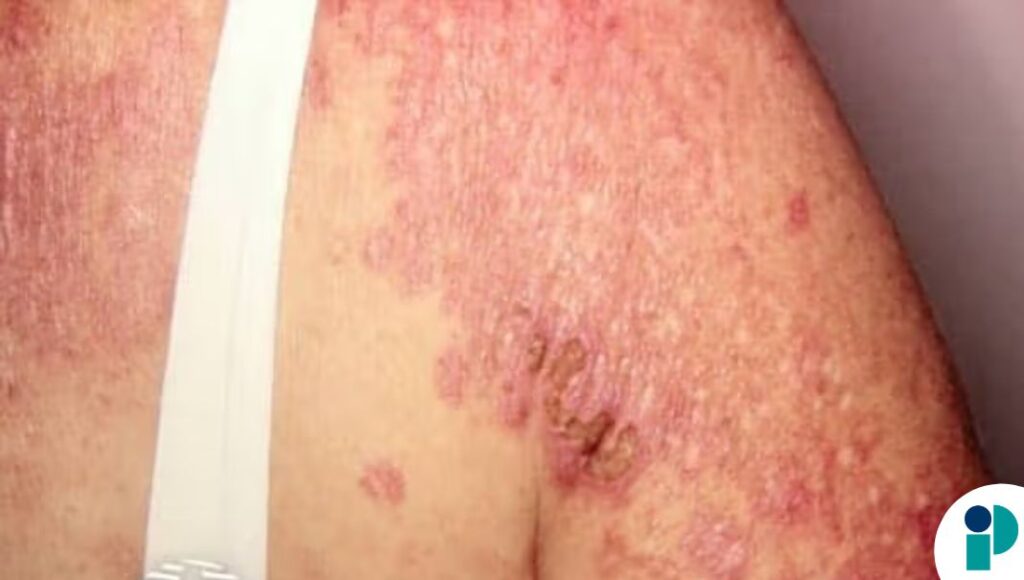
La dermatomiositis es una enfermedad autoinmune caracterizada por inflamación muscular y manifestaciones cutáneas, que con frecuencia puede asociarse con enfermedad pulmonar intersticial, mayor riesgo de malignidad y exposición prolongada a corticosteroides.
La actividad persistente de la enfermedad y el daño acumulado en órganos contribuyen a limitaciones funcionales, comorbilidades y deterioro de la calidad de vida, lo que resalta la necesidad de tratamientos dirigidos que permitan controlar la inflamación sin depender de altas dosis de esteroides.
“La comunidad médica y los pacientes con dermatomiositis han esperado durante décadas terapias innovadoras que apunten directamente a la biología subyacente de la enfermedad”, señaló la Dra. Ruth Ann Vleugels, especialista en dermatología y enfermedades autoinmunes cutáneas en Mass General Brigham y profesora en Harvard Medical School.
Resultados del ensayo clínico
La decisión de la FDA se sustenta en los resultados del ensayo clínico fase 3 VALOR, considerado el estudio intervencional más grande y prolongado realizado hasta la fecha en dermatomiositis, así como el primer ensayo positivo controlado con placebo con seguimiento de 52 semanas.
El estudio se llevó a cabo en 90 centros a nivel mundial, donde los participantes fueron asignados aleatoriamente para recibir brepocitinib 30 mg, brepocitinib 15 mg o placebo.
Al finalizar el periodo de seguimiento, la dosis de 30 mg de brepocitinib logró mejoras estadísticamente significativas y clínicamente relevantes frente al placebo en el Myositis Total Improvement Score (TIS), el criterio principal del estudio que integra seis medidas centrales de actividad de la enfermedad. La diferencia frente al placebo se observó desde la semana 4 y se mantuvo durante todo el estudio.
Además, esta dosis cumplió los nueve criterios secundarios clave, incluyendo mejoras en la enfermedad cutánea, la fuerza muscular y la reducción del uso de corticosteroides.
Potencial efecto ahorrador de esteroides
Más de dos tercios de los pacientes tratados con brepocitinib 30 mg alcanzaron un TIS40, considerado el doble del umbral mínimo clínicamente significativo.
Al inicio del estudio, aproximadamente el 75 % de los participantes utilizaban corticosteroides, con una dosis promedio cercana a 12 mg diarios.
Entre los pacientes que recibieron brepocitinib:
- 62 % logró reducir la dosis de esteroides a ≤2,5 mg diarios a las 52 semanas (frente a 34 % con placebo).
- 42 % pudo suspender completamente el uso de esteroides (en comparación con 23 % en el grupo placebo).
Estos resultados sugieren un potencial efecto ahorrador de esteroides, un objetivo importante en el manejo de esta enfermedad debido a las complicaciones asociadas al uso prolongado de estos medicamentos.
Un posible cambio en el tratamiento de la enfermedad
Para los especialistas que tratan enfermedades autoinmunes del tejido conectivo, la decisión pendiente de la FDA podría representar un avance importante en un campo donde las opciones terapéuticas siguen siendo limitadas.
“El estudio fase 3 sugiere que esta terapia tiene el potencial de mejorar de forma significativa la calidad de vida y la función de los pacientes con una terapia oral administrada una vez al día”, afirmó la Dra. Vleugels.
Por su parte, Ben Zimmer, director ejecutivo de Priovant, señaló que la aceptación de la solicitud por parte de la FDA representa un paso importante hacia el objetivo de ofrecer nuevas opciones terapéuticas para pacientes con dermatomiositis que aún enfrentan necesidades médicas no cubiertas.
Fuente original aquí