La Administración de Alimentos y Medicamentos de Estados Unidos (FDA) ha aprobado una modificación en el esquema de dosificación del medicamento Kisunla, desarrollado por Eli Lilly para el tratamiento del Alzheimer en etapa temprana, con el objetivo de reducir los riesgos de inflamación cerebral asociados al fármaco.
Kisunla, administrado mediante infusión mensual, fue aprobado hace poco más de un año tras demostrar en estudios clínicos que podía retrasar en un 29 % la progresión del deterioro cognitivo en comparación con placebo. Pertenece a una clase de medicamentos diseñados para eliminar del cerebro la proteína beta amiloide, relacionada con el desarrollo del Alzheimer.
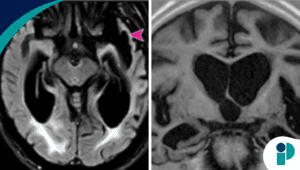
Sin embargo, la FDA había incluido su advertencia de seguridad más fuerte en la etiqueta del medicamento, debido al riesgo de desarrollar ARIA-E, un tipo de inflamación cerebral potencialmente peligrosa. Datos presentados por Lilly mostraron que el 24% de los pacientes que siguieron el esquema estándar de dosificación experimentaron ARIA-E, frente a solo el 14% de los que recibieron una dosificación gradual.
Ante esto, la agencia reguladora ha aprobado el cambio en el protocolo de administración, que ahora recomienda comenzar con un solo vial de Kisunla y añadir un vial adicional cada mes, hasta alcanzar la dosis completa de cuatro viales al cuarto mes. En el esquema anterior, se iniciaba con dos viales mensuales desde la primera aplicación.
«La actualización ayudará a los profesionales de la salud en su evaluación de las opciones de tratamiento para los pacientes y en sus análisis de beneficios y riesgos», declaró la doctora Brandy Matthews, vicepresidenta de Lilly para asuntos médicos globales y estadounidenses para la enfermedad de Alzheimer.
Lilly aseguró que el nuevo esquema de dosificación no compromete la capacidad del medicamento para reducir las placas de amiloide en el cerebro, uno de los marcadores característicos del Alzheimer.
Kisunla compite directamente con Leqembi, el fármaco de Eisai y Biogen, también aprobado para tratar el Alzheimer en etapas iniciales y que incluye advertencias similares sobre el riesgo de ARIA-E. Ambos tratamientos requieren diagnósticos previos por imágenes cerebrales y seguimiento continuo, lo que ha dificultado su adopción generalizada en el sistema de salud.
Actualmente, tanto Kisunla como Leqembi están siendo evaluados en ensayos clínicos en pacientes aún asintomáticos, con la esperanza de ofrecer tratamientos preventivos antes del inicio del deterioro cognitivo.
Según la Asociación de Alzheimer de Estados Unidos, más de 6 millones de personas viven con esta enfermedad en el país, una cifra que se espera continúe creciendo en las próximas décadas, alimentando la urgencia de desarrollar terapias efectivas y seguras.
Fuente consultada: AQUÍ