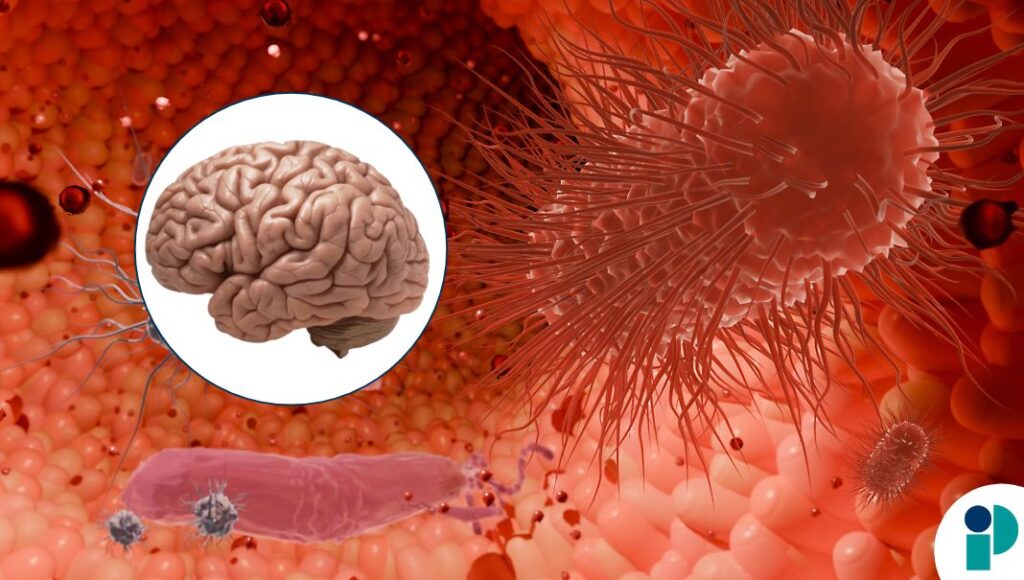
Investigadores de la Case Western Reserve University identificaron una conexión directa entre bacterias intestinales y el deterioro cerebral en pacientes con Esclerosis Lateral Amiotrófica (ELA) y Demencia Frontotemporal (DFT), dos de las enfermedades neurodegenerativas más agresivas.
El hallazgo, publicado recientemente en la revista Cell Reports, describe cómo ciertos azúcares bacterianos desencadenan respuestas inmunitarias que terminan destruyendo células del cerebro, abriendo nuevas posibilidades terapéuticas.
¿Cómo afectan la ELA y la DFT al cerebro?
La demencia frontotemporal compromete principalmente los lóbulos frontal y temporal, provocando cambios en:
- Personalidad
- Conducta
- Lenguaje
Por su parte, la ELA afecta las neuronas motoras, lo que produce:
- Debilidad muscular progresiva
- Pérdida de movilidad
- Parálisis
Aunque existen factores asociados como genética, ambiente, traumatismos y dieta—, la mayoría de los casos aún no tiene una causa claramente definida.
El papel inesperado de las bacterias intestinales
El equipo descubrió que bacterias intestinales dañinas producen formas inflamatorias de glucógeno (un tipo de azúcar).
Estas moléculas:
- Activan el sistema inmunitario.
- Generan inflamación.
- Desencadenan daño neuronal.
“Encontramos que bacterias intestinales nocivas producen formas inflamatorias de glucógeno, y que estos azúcares desencadenan respuestas inmunitarias que dañan el cerebro”, explicó Aaron Burberry, investigador principal del estudio.
Datos clave del estudio
- Se analizaron 23 pacientes con ELA/DFT.
- 70 % presentaba niveles peligrosos de glucógeno bacteriano.
- Entre personas sin estas enfermedades, solo un tercio tenía niveles elevados.
Esto sugiere que estos azúcares microbianos podrían actuar como factor desencadenante del daño cerebral.
Implicaciones clínicas inmediatas
El descubrimiento ofrece dos aplicaciones relevantes:
1. Nuevas dianas terapéuticas
Permite desarrollar tratamientos dirigidos a:
- Descomponer azúcares dañinos en el intestino.
- Modular la microbiota intestinal.
2. Biomarcadores diagnósticos
Los niveles de glucógeno bacteriano podrían ayudar a:
- Identificar pacientes en riesgo.
- Seleccionar candidatos para terapias dirigidas al intestino.
El equipo también probó reducir estos azúcares dañinos. Según Alex Rodriguez-Palacios, investigador del Digestive Health Research Institute: La disminución de los azúcares perjudiciales “mejoró la salud cerebral y extendió la esperanza de vida” en modelos experimentales.
El hallazgo es especialmente relevante para portadores de la mutación C9ORF72, la causa genética más común de ELA y DFT.
El estudio explica por qué:
- Algunas personas con la mutación desarrollan la enfermedad.
- Otras nunca presentan síntomas.
La diferencia podría estar en la composición de sus bacterias intestinales, señalando al microbioma como desencadenante ambiental clave.
Modelos experimentales únicos
La investigación fue posible gracias a modelos de ratones libres de gérmenes, criados en entornos completamente estériles.
Estos sistemas permiten:
- Introducir bacterias específicas.
- Observar su efecto directo en el cerebro.
El programa es liderado por el Digestive Health Research Institute bajo la dirección de Fabio Cominelli, utilizando un innovador sistema de alojamiento estéril “cage-in-cage”, disponible en pocas instituciones del mundo.
Próximos pasos: ensayos clínicos en el horizonte
Los investigadores planean:
- Estudios más amplios del microbioma en pacientes antes y después del inicio de la enfermedad.
- Ensayos clínicos para evaluar si degradar el glucógeno bacteriano puede ralentizar la progresión.
Según Burberry, estos estudios podrían comenzar en aproximadamente un año.
Una nueva esperanza terapéutica
Este descubrimiento refuerza la creciente evidencia sobre el eje intestino-cerebro y su papel en enfermedades neurológicas.
Al intervenir sobre bacterias intestinales y sus metabolitos, la ciencia podría abrir una vía terapéutica innovadora para patologías que, hasta ahora, tienen opciones de tratamiento muy limitadas.
Fuente original aquí