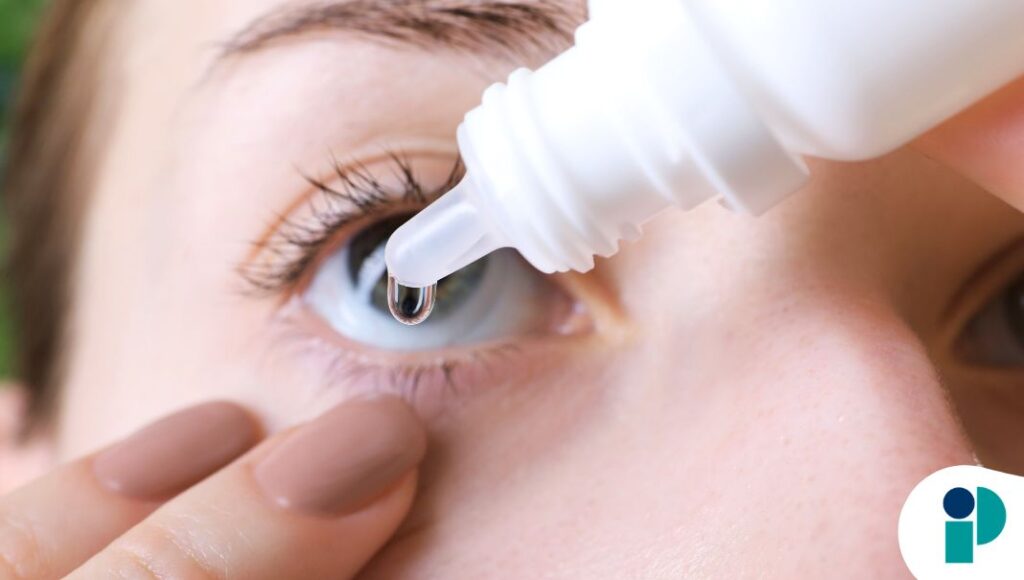
La Administración de Alimentos y Medicamentos (FDA) anunció el retiro voluntario de más de 3 millones de frascos de gotas oftálmicas de venta libre debido a preocupaciones relacionadas con la seguridad del producto, específicamente por una posible “falta de garantía de esterilidad”.
Los productos son fabricados por KC Pharmaceuticals, con sede en Pomona, California, y se comercializan bajo diversas marcas en importantes cadenas minoristas.
Productos distribuidos en grandes cadenas comerciales
Las gotas oftálmicas retiradas se vendían ampliamente en tiendas como CVS Pharmacy, Walgreens y Rite Aid, lo que amplía el alcance potencial de los consumidores afectados.
Entre los productos incluidos en el retiro se encuentran:
- Gotas oftálmicas estériles AC
- Gotas oftálmicas Advanced Relief
- Gotas para el alivio de la sequedad ocular
- Gotas oftálmicas ultra lubricantes
- Fórmula original estéril
- Gotas lubricantes para el enrojecimiento
- Gotas para aliviar las lágrimas
- Lágrimas artificiales lubricantes estériles
Estos productos contienen ingredientes como tetrahidrozolina, polietilenglicol, glicerina, hipromelosa y povidona, utilizados comúnmente para tratar la resequedad ocular y el enrojecimiento.
La FDA clasificó esta acción como una retirada de Clase II, lo que implica que el uso del producto podría causar efectos adversos temporales o médicamente reversibles, aunque el riesgo de consecuencias graves es bajo. Hasta el momento, no se han reportado lesiones ni efectos adversos asociados con el uso de estas gotas oftálmicas.
¿Qué implica la falta de esterilidad?
La esterilidad es un requisito crítico en productos oftálmicos, ya que cualquier contaminación puede aumentar el riesgo de infecciones oculares. Aunque no se han confirmado casos, la ausencia de esta garantía llevó a tomar la medida preventiva.
De acuerdo con la FDA, en situaciones de retiro Clase II, los consumidores pueden continuar usando el producto, a menos que el fabricante indique lo contrario. Sin embargo, se recomienda precaución y estar atentos a nuevas actualizaciones.
Hasta ahora, no se han dado a conocer detalles específicos sobre qué originó el problema de esterilidad. La empresa fabricante no ha emitido declaraciones públicas tras el anuncio.
Recomendaciones para los consumidores:
- Verificar si el producto adquirido hace parte del lote retirado
- Suspender su uso ante cualquier síntoma ocular inusual
- Consultar a un profesional de la salud en caso de irritación, dolor o enrojecimiento persistente
- Seguir las actualizaciones oficiales de la FDA