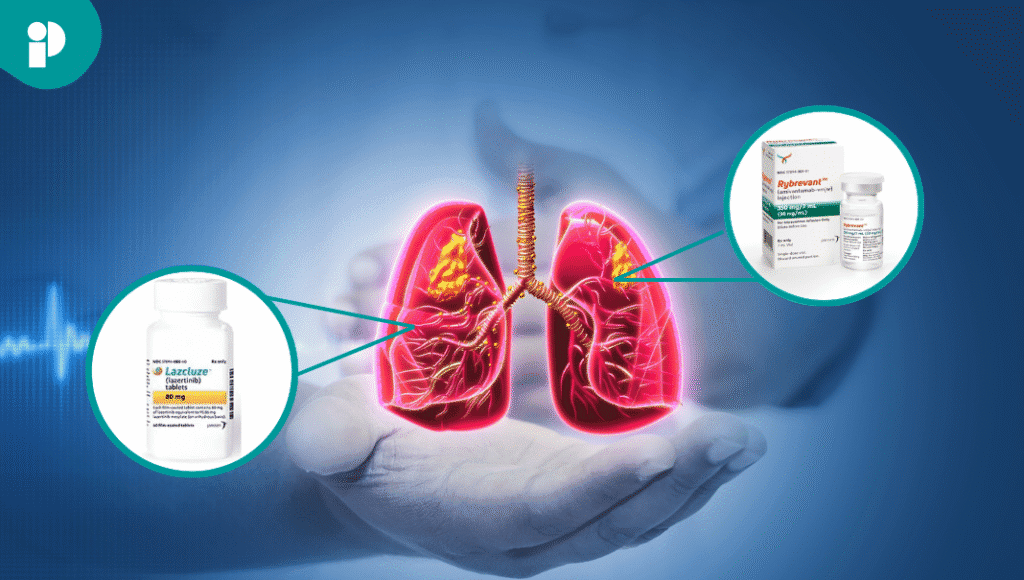
La Comisión Europea ha aprobado este lunes la autorización de comercialización para Lazcluze (lazertinib) en combinación con RYbrevant (amivantamab), un nuevo régimen terapéutico destinado a pacientes adultos con cáncer de pulmón no microcítico (CPNM) avanzado con mutaciones específicas en el receptor del factor de crecimiento epidérmico (EGFR).
Esta aprobación abre la puerta a un tratamiento que podría prolongar la supervivencia en una mediana de un año o más frente a las terapias actuales.
Respaldada por los resultados del estudio fase 3 MARIPOSA, la terapia combinada mostró mejoras estadísticamente y clínicamente significativas tanto en supervivencia libre de progresión (SLP) como en supervivencia global (SG), comparada con el estándar actual, osimertinib en monoterapia.
Estos resultados se presentaron inicialmente en el Congreso de la Sociedad Europea de Oncología Médica (ESMO) 2023 y fueron reforzados con datos a largo plazo en la Conferencia Mundial sobre Cáncer de Pulmón 2024.
“El tratamiento en primera línea con amivantamab y lazertinib representa un avance crucial para pacientes con CPNM con mutaciones en EGFR no tratados, ofreciendo un régimen sin quimioterapia que mejora la esperanza de vida”, señaló Antonio Passaro, oncólogo médico del Instituto Europeo de Oncología de Milán.
La terapia ha demostrado un perfil de seguridad consistente con estudios previos, con efectos adversos mayoritariamente leves o moderados (grado 1 o 2), como paroniquia (68%), reacciones a la perfusión (63%) y erupción cutánea (62%). Los efectos adversos graves más frecuentes incluyeron erupción cutánea (15%) y embolia pulmonar (8%), con una tasa de interrupción del tratamiento del 10 %.
Henar Hevia, directora del Área de Oncología para Europa, África y Oriente Medio de Johnson & Johnson Innovative Medicine, destacó que la tasa de supervivencia a cinco años para estos pacientes es actualmente inferior al 20%, lo que subraya la importancia de contar con nuevas opciones terapéuticas.
Por último, ha comunicado que la aprobación de hoy marca “un momento importante en la atención del cáncer de pulmón”, brindando una nueva opción a los pacientes a través de un régimen sin quimioterapia, ofreciéndoles, eventualmente, más tiempo con sus seres queridos.
Esta decisión sigue a la aprobación, en diciembre de 2024, de una extensión de indicación para el anticuerpo biespecífico amivantamab, también en combinación con lazertinib, consolidando el potencial transformador de esta terapia en el tratamiento del cáncer de pulmón con mutaciones en EGFR.
Fuente consultada: AQUÍ